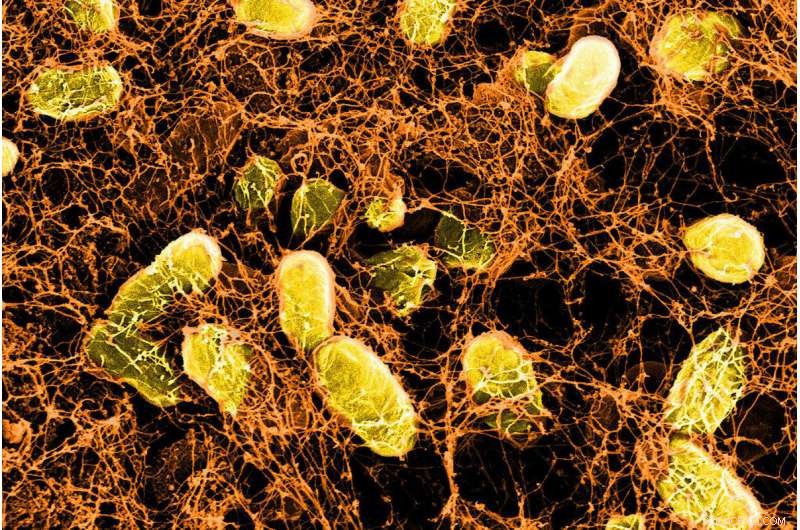
Imagen microscópica de un hidrogel bacteriano que se une a proteínas mucosas en la superficie de la pared intestinal. Crédito:Instituto Wyss de la Universidad de Harvard
Las heridas externas, como cortes en la piel o abrasiones, a menudo se pueden cubrir fácilmente con una curita simple o un parche para heridas más grande para protegerlas y facilitar su curación. Cuando se trata de algunas superficies internas como las del intestino que están recubiertas con una capa de moco, sin embargo, tales materiales de cicatrización de heridas convencionales son ineficaces porque el moco dificulta su fijación firme y los aleja rápidamente del lugar de la herida.
Ahora, Investigadores del Instituto Wyss de Ingeniería Biológicamente Inspirada de Harvard y la Escuela de Ingeniería y Ciencias Aplicadas John A. Paulson (SEAS) han desarrollado una solución a este problema en forma de hidrogeles probióticos hechos de nanofibras mucoadhesivas y producidos por una bacteria intestinal natural diseñada. Los hidrogeles se pueden producir fácilmente a partir de cultivos bacterianos y se pueden aplicar como "geles vivos" autoregeneradores de vida más larga o "geles sin células" de vida más corta a las superficies intestinales mediante jeringas. rociar, y técnicas endoscópicas para proporcionar un sello. El estudio se publica en Materiales avanzados .
"Este nuevo tipo de material vivo diseñado con su facilidad de producción y almacenamiento, biocompatibilidad, y las propiedades mucoadhesivas podrían abrir la puerta a las estrategias bioactivas de curación de heridas para su uso dentro de la luz del intestino humano, "dijo Neel Joshi, quien es un miembro principal de la facultad en el Instituto Wyss y profesor asociado en SEAS. "Básicamente, podemos programar la maquinaria molecular normal productora de nanofibras de materiales no patógenos E. coli para producir hidrogeles que tienen una viscosidad muy parecida a la del moco, y con capacidades mucoadhesivas incorporadas; y su modularidad podría permitirnos ajustarlos para que coincidan con secciones específicas del tracto gastrointestinal con sus composiciones y estructuras de moco individuales ".
Joshi y otros laboratorios han aprovechado previamente cepas comensales de E. coli para secretar nanofibras formadoras de biopelículas, y como fundiciones vivientes para la fabricación de productos farmacéuticos, productos químicos finos, o sustancias que pueden ayudar con la remediación ambiental mediante la ingeniería de la proteína CsgA que secretan las bacterias, que se autoensambla en nanofibras curli en el entorno extracelular. En estas aplicaciones pasadas, CsgA se modificó para permitir funciones enzimáticas o estructurales adicionales, como la realización de una reacción química necesaria para la síntesis de un fármaco o sustancia química. Sin embargo, Los materiales a base de nanofibras de curli hasta ahora no se han desarrollado para uso directo como terapéuticos.
"Se sabe que las biopelículas producidas naturalmente obstaculizan los procesos de cicatrización de heridas hasta un punto en el que necesitan ser gestionadas activamente por los profesionales de la salud. Básicamente, hemos pirateado una de las maquinarias centrales que las produce con el objetivo a largo plazo de hacer exactamente lo contrario , para producir materiales que puedan ayudar a la cicatrización de heridas en un entorno que es inaccesible para otros materiales, "dijo la primera autora Anna Duraj-Thatte, quien es becario postdoctoral de la Escuela de Graduados en Artes y Ciencias en el equipo de Joshi.
Para permitir la formación de hidrogeles extracelulares, los investigadores programaron una cepa no patógena de la bacteria intestinal E. coli para sintetizar una variante de la proteína CsgA curli que se fusiona con el dominio de unión al moco de los factores del trébol humano (TFF). Los TFF son co-secretados por células productoras de moco para proteger el epitelio de la mucosa de una variedad de agresiones, y ayúdelos a reparar lesiones. Un simple paso de filtración permite la separación limpia del hidrogel que contiene bacterias vivas del resto del cultivo, mientras que los geles sin células requieren un paso adicional en el que las bacterias mueren con un simple tratamiento químico. "Creemos que la presencia de los dominios TFF permite que diferentes fibras rizadas se reticulen entre sí y formen una malla de almacenamiento de agua, y demostró que las propiedades exactas del hidrogel dependen del tipo de TFF utilizado, "dijo Duraj-Thatte.
Colaborando con Jeffrey Karp y el instructor de medicina Yuhan Lee en Brigham and Women's Hospital, el equipo probó la especificidad de la adhesión tisular en función del tipo de dominios adjuntos en el hidrogel. Cuando se presentaron TFF en los hidrogeles, mejoraron la adhesión sólo a la superficie mucosa expuesta a la luz de una muestra de tejido de colon de cabra. Alternativamente, cuando un dominio se une a la proteína fibronectina, que no se encuentra en la mucosa, but on the outward-facing serosal surface of the colon—the hydrogels instead preferentially stuck to the serosal side of the colon tissue sample.
"Since hydrogels with different TFF domains can be easily sprayed onto tissue surfaces with controllable adhesion and functional activity, we envision their potential use in endoscopic procedures to treat intestinal disorders, like a spray-on bandage, " said Karp, who is a professor of medicine at Brigham and Women's Hospital and Harvard Medical School.
When given orally to mice, the cell-containing live gels could withstand the harsh pH and digestive conditions of the stomach and small intestine to reach the cecum with the bacteria intact. The team also found that hydrogels bearing one particular TFF domain (TFF2) enhanced retention of the material in the colon. "The presence of bacteria in live gels prolonged their residency times in the gut from one day to at least five days due to the bacteria's ability to continuously regenerate the curli fiber networks that are decorated with TFFs, without affecting the health of mice in any obvious way, " said Joshi.
"This is a great example of synthetic biology-based jujutsu in which Joshi's team took a major problem created by bacteria—the biofilms they create that are so difficult to access and remove—and then flipped the problem on its head through genetic engineering so that the biofilm now essentially becomes a healing Band-aid for our gut. It's an amazing example of biologically inspired engineering at its best, " said Wyss Director Donald Ingber, the Judah Folkman Professor of Vascular Biology at HMS and the Vascular Biology Program at Boston Children's Hospital, as well as professor of bioengineering at SEAS.
This story is published courtesy of the Harvard Gazette, Harvard University's official newspaper. For additional university news, visit Harvard.edu.