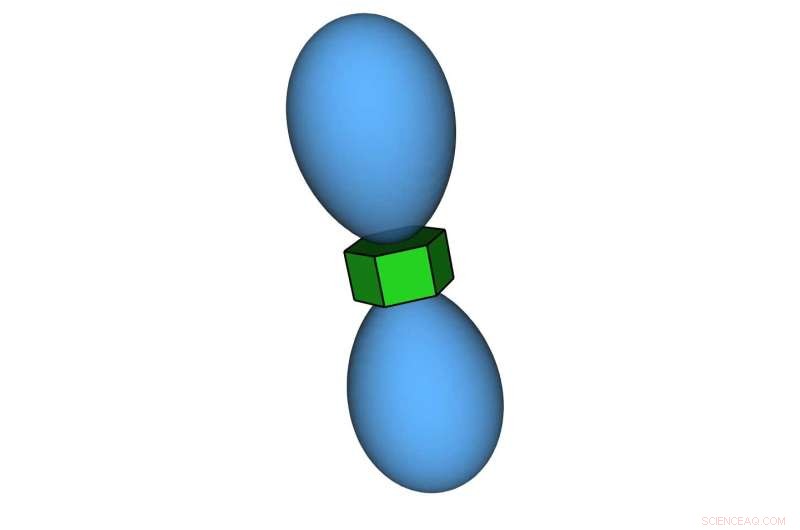
Nanopartículas en forma de prisma orbital. La densidad de las pseudopartículas alrededor de las nanopartículas se asemeja a la densidad electrónica en los orbitales electrónicos de los átomos. Crédito:Thi Vo, Glotzer Group, Universidad de Michigan
La entropía, una propiedad física a menudo explicada como "desorden", se revela como creadora de orden con una nueva teoría de enlace desarrollada en la Universidad de Michigan y publicada en las Proceedings of the National Academy of Sciences. .
Los ingenieros sueñan con usar nanopartículas para construir materiales de diseño, y la nueva teoría puede ayudar a guiar los esfuerzos para hacer que las nanopartículas se ensamblen en estructuras útiles. La teoría explica los resultados anteriores que exploran la formación de estructuras cristalinas mediante nanopartículas de espacio restringido, lo que permite cuantificar y aprovechar la entropía en futuros esfuerzos.
Y, curiosamente, el conjunto de ecuaciones que gobiernan las interacciones de las nanopartículas debido a la entropía reflejan las que describen los enlaces químicos. Sharon Glotzer, directora del Departamento de Ingeniería Química Anthony C. Lembke, y Thi Vo, investigadora posdoctoral en ingeniería química, respondieron algunas preguntas sobre su nueva teoría.
¿Qué es el enlace entrópico?
Glotzer:"El enlace entrópico es una forma de explicar cómo interactúan las nanopartículas para formar estructuras cristalinas. Es análogo a los enlaces químicos formados por los átomos. Pero, a diferencia de los átomos, no hay interacciones de electrones que mantienen unidas a estas nanopartículas. En cambio, la atracción surge debido a entropía."
"A menudo, la entropía se asocia con el desorden, pero en realidad se trata de opciones. Cuando las nanopartículas se amontonan y las opciones son limitadas, resulta que la disposición más probable de las nanopartículas puede ser una estructura cristalina particular. Esa estructura le da al sistema la mayor cantidad de opciones. , y por lo tanto la entropía más alta. Grandes fuerzas entrópicas surgen cuando las partículas se acercan unas a otras".
"Al realizar los estudios más extensos sobre las formas de las partículas y los cristales que forman, mi grupo descubrió que a medida que cambia la forma, cambia la direccionalidad de esas fuerzas entrópicas que guían la formación de estas estructuras cristalinas. Esa direccionalidad simula un enlace y dado que está impulsado por la entropía, lo llamamos enlace entrópico".
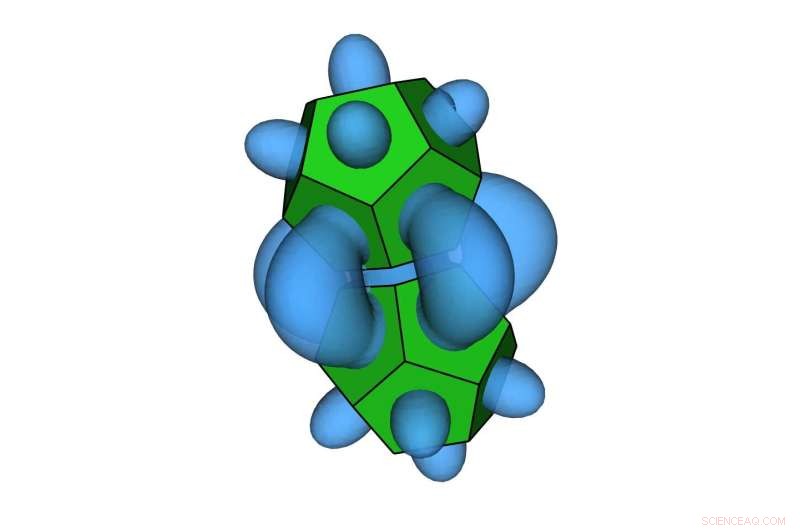
Nanopartículas en forma de dodecaedro. Esta nueva forma de entender cómo la entropía crea fuerzas atractivas entre nanopartículas podría acelerar el desarrollo de nanomateriales con propiedades diseñadas. Crédito:Thi Vo, Glotzer Group, Universidad de Michigan
¿Por qué es importante?
Glotzer:"La contribución de la entropía a la creación de orden a menudo se pasa por alto cuando se diseñan nanopartículas para el autoensamblaje, pero eso es un error. Si la entropía está ayudando a su sistema a organizarse, es posible que no necesite diseñar una atracción explícita entre partículas, por ejemplo, usando ADN o otras moléculas pegajosas, con una interacción tan fuerte como pensabas. Con nuestra nueva teoría, podemos calcular la fuerza de esos enlaces entrópicos".
"Si bien sabíamos que las interacciones entrópicas pueden ser direccionales como enlaces, nuestro avance es que podemos describir esos enlaces con una teoría que, línea por línea, coincide con la teoría que escribiría para las interacciones de electrones en enlaces químicos reales. Eso es profundo. Me sorprende que incluso sea posible hacer eso. Hablando matemáticamente, pone los enlaces químicos y los enlaces entrópicos en el mismo plano. Esto es fundamentalmente importante para nuestra comprensión de la materia y prácticamente importante para hacer nuevos materiales".
Sin embargo, los electrones son la clave de esas ecuaciones químicas. ¿Cómo hiciste esto cuando ninguna partícula media en las interacciones entre tus nanopartículas?
Glotzer:"La entropía está relacionada con el espacio libre en el sistema, pero durante años no sabía cómo contar ese espacio. La gran idea fue que podíamos contar ese espacio usando partículas puntuales ficticias. Y eso nos dio el análogo matemático de los electrones."
Vo:"Las pseudopartículas se mueven alrededor del sistema y llenan los espacios que son difíciles de llenar para otra nanopartícula; a esto lo llamamos el volumen excluido alrededor de cada nanopartícula. A medida que las nanopartículas se vuelven más ordenadas, el volumen excluido alrededor de ellas se vuelve más pequeño y el la concentración de pseudopartículas en esas regiones aumenta. Los enlaces entrópicos son donde esa concentración es más alta".
"En condiciones de hacinamiento, la entropía perdida al aumentar el orden se ve compensada por la entropía ganada al reducir el volumen excluido. Como resultado, la configuración con la entropía más alta será aquella en la que las pseudopartículas ocupen el menor espacio". Estudio revela cómo romper la simetría en cristales coloidales