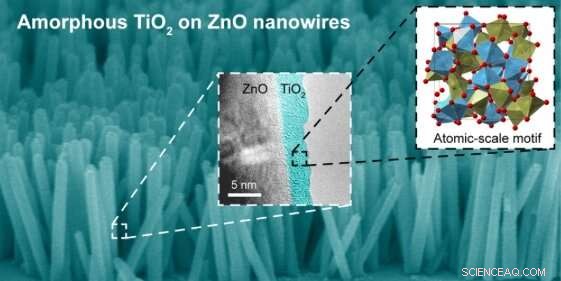
(Fondo) Una imagen de microscopio electrónico de barrido de color falso de nanocables de óxido de zinc (ZnO) recubiertos con dióxido de titanio, o titania (TiO2). De media, los nanocables son 10 veces más largos que anchos. El recuadro de rayas blancas contiene una imagen de microscopio electrónico de transmisión de alta resolución que distingue entre el núcleo de ZnO y la capa de titania. El recuadro con rayas negras presenta un modelo estructural de la cáscara de titania amorfa, con los círculos rojos correspondientes a los átomos de oxígeno y los poliedros verde y azul correspondientes a los átomos de titanio coordinados y subcoordinados, respectivamente. Crédito:Laboratorio Nacional Brookhaven
La energía solar recolectada por semiconductores —materiales cuya resistencia eléctrica se encuentra entre la de los metales comunes y los aislantes— puede desencadenar reacciones electroquímicas en la superficie para generar combustibles limpios y sostenibles como el hidrógeno. Se necesitan catalizadores altamente estables y activos para acelerar estas reacciones, especialmente para dividir las moléculas de agua en oxígeno e hidrógeno. Los científicos han identificado varios semiconductores fuertes que absorben la luz como catalizadores potenciales; sin embargo, debido a la fotocorrosión, muchos de estos catalizadores pierden su actividad por la reacción de disociación del agua. Corrosión inducida por la luz, o fotocorrosión, ocurre cuando el catalizador mismo sufre reacciones químicas (oxidación o reducción) a través de portadores de carga (electrones y "huecos, "o electrones faltantes) generados por la excitación de la luz. Esta degradación limita la actividad catalítica.
Ahora, Científicos del Centro de Nanomateriales Funcionales (CFN), una instalación para usuarios de la Oficina de Ciencias Científicas del Departamento de Energía de EE. UU. (DOE) en el Laboratorio Nacional de Brookhaven, han ideado una técnica para optimizar la actividad de uno de estos catalizadores:500 nanómetros de longitud pero nanoestructuras relativamente delgadas (40 a 50 nanómetros) con apariencia de alambre, o nanocables, hecho de óxido de zinc (ZnO). Su técnica, descrita en un artículo publicado en línea en Nano letras el 3 de mayo:implica el tratamiento químico de la superficie de los nanocables de tal manera que puedan recubrirse uniformemente con una película ultrafina (de dos a tres nanómetros de espesor) de dióxido de titanio (titania), que actúa como catalizador y capa protectora.
La investigación dirigida por CFN es una colaboración entre la Fuente de luz sincrotrón nacional II (NSLS-II) de Brookhaven Lab —otra instalación para usuarios de la Oficina de ciencia del DOE— y la Iniciativa de ciencia computacional (CSI); el Centro de Ciencia de Materiales Computacionales en el Laboratorio de Investigación Naval; y el Departamento de Ciencia de Materiales e Ingeniería Química de la Universidad de Stony Brook.

(Sentado de frente) Iradwikanari Waluyo, Mingzhao Liu, Dario Stacchiola, (de pie desde el frente) Mehmet Topsakal, Mark Hybertsen, Deyu Lu, y Eli Stavitski en la línea de luz de espectroscopia de capa interna de la fuente de luz sincrotrón nacional II de Brookhaven Lab (NSLS-II). Los científicos realizaron experimentos de espectroscopía de absorción de rayos X en NSLS-II para caracterizar el estado químico de los recubrimientos de dióxido de titanio (titania) en nanocables de óxido de zinc. Procesaron químicamente los nanocables para fabricar los recubrimientos, que aumentan la eficiencia de los nanocables para catalizar la reacción de división del agua que produce oxígeno e hidrógeno. un combustible sostenible, más propenso a adherirse. Estos resultados de caracterización se combinaron con imágenes de microscopía electrónica y análisis teóricos para generar un modelo de la estructura atómica amorfa (no cristalina) de titania. Crédito:Laboratorio Nacional Brookhaven
"Los nanocables son estructuras catalizadoras ideales porque tienen una gran superficie para absorber la luz, y ZnO es un material abundante en la tierra que absorbe fuertemente la luz ultravioleta y tiene una alta movilidad de electrones. "dijo el coautor correspondiente y líder del estudio Mingzhao Liu, un científico en el CFN Interface Science and Catalysis Group. "Sin embargo, por ellos mismos, Los nanocables de ZnO no tienen suficiente actividad catalítica o estabilidad para la reacción de división del agua. Recubriéndolos uniformemente con películas ultrafinas de titania, otro material de bajo costo que es químicamente más estable y más activo para promover la transferencia de carga interfacial, mejora estas propiedades para aumentar la eficiencia de la reacción en un 20 por ciento en comparación con los nanocables de ZnO puro ".
Para "mojar" la superficie de los nanocables para el recubrimiento de titania, los científicos combinaron dos métodos de procesamiento de superficies:recocido térmico y pulverización catódica con plasma a baja presión. Para el recocido térmico, calentaron los nanocables en un ambiente de oxígeno para eliminar defectos y contaminantes; para la pulverización de plasma, bombardearon los nanocables con iones de gas oxígeno energético (plasma), que expulsó átomos de oxígeno de la superficie de ZnO.
"Estos tratamientos modifican la química de la superficie de los nanocables de tal manera que es más probable que el recubrimiento de titania se adhiera durante la deposición de la capa atómica". "explicó Liu." En la deposición de la capa atómica, diferentes precursores químicos reaccionan con la superficie de un material de manera secuencial para formar películas delgadas con una capa de átomos a la vez ".
Los científicos tomaron imágenes de las estructuras de la capa de nanocables con microscopios electrónicos de transmisión en el CFN, hacer brillar un haz de electrones a través de la muestra y detectar los electrones transmitidos. Sin embargo, porque la capa ultrafina de titania no es cristalina, necesitaban utilizar otros métodos para descifrar su estructura "amorfa". Realizaron experimentos de espectroscopía de absorción de rayos X en dos líneas de luz NSLS-II:espectroscopía de capa interna (ISS) y espectroscopía de rayos X in situ y Operando Soft (IOS).
"Las energías de rayos X en las dos líneas de luz son diferentes, por lo que los rayos X interactúan con diferentes niveles electrónicos en los átomos de titanio, "dijo el coautor Eli Stavitski, Físico de la línea de luz de la ISS. "Los espectros de absorción complementarios generados a través de estos experimentos confirmaron la estructura altamente amorfa de titania, con dominios cristalinos limitados a unos pocos nanómetros. Los resultados también nos dieron información sobre el estado de valencia (carga) de los átomos de titanio (cuántos electrones hay en la capa más externa que rodea el núcleo) y la esfera de coordinación. o el número de átomos de oxígeno vecinos más cercanos ".
Luego, los teóricos y científicos computacionales del equipo determinaron la estructura atómica más probable asociada con estos espectros experimentales. En materiales con estructura cristalina, la disposición de un átomo y sus vecinos es la misma en todo el cristal. Pero las estructuras amorfas carecen de esta uniformidad u orden de largo alcance.
"Tuvimos que averiguar la combinación correcta de configuraciones estructurales responsables de la naturaleza amorfa del material, "explicó el coautor correspondiente, Deyu Lu, científico del Grupo de Teoría y Computación CFN. "Primero, Examinamos una base de datos estructural existente e identificamos más de 300 estructuras locales relevantes utilizando herramientas de análisis de datos desarrolladas previamente por el ex postdoctorado de CFN Mehmet Topsakal y el científico computacional de CSI Shinjae Yoo. Calculamos los espectros de absorción de rayos X para cada una de estas estructuras y seleccionamos 11 representativos como funciones de base para ajustar nuestros resultados experimentales. De este análisis, determinamos el porcentaje de átomos de titanio con una coordinación local particular ".
El análisis mostró que aproximadamente la mitad de los átomos de titanio estaban "subcoordinados". En otras palabras, estos átomos de titanio estaban rodeados por solo cuatro o cinco átomos de oxígeno, a diferencia de las estructuras en las formas más comunes de titania, que tienen seis átomos de oxígeno vecinos.
Para validar el resultado teórico, Lu y los otros teóricos:Mark Hybertsen, líder del Grupo de Teoría y Computación CFN; Sencer Selcuk, postdoctorado de CFN; y el ex postdoctorado de CFN John Lyons, ahora un científico físico en el Laboratorio de Investigación Naval, creó un modelo a escala atómica de la estructura amorfa de titania. Aplicaron la técnica computacional de dinámica molecular para simular el proceso de recocido que produjo la estructura amorfa. Con este modelo, también calcularon el espectro de absorción de rayos X de titania; sus cálculos confirmaron que alrededor del 50 por ciento de los átomos de titanio estaban subcoordinados.
"Estos dos métodos independientes nos dieron un mensaje coherente sobre la estructura local de titania, "dijo Lu.
"Los átomos completamente coordinados no son muy activos porque no pueden unirse a las moléculas con las que hacen química en las reacciones, ", explicó Stavitski." Para hacer que los catalizadores sean más activos, necesitamos reducir su coordinación ".
"El comportamiento del transporte de titania amorfa es muy diferente al de titania a granel, "agregó Liu." La titania amorfa puede transportar eficientemente tanto huecos como electrones como portadores de carga activa, que impulsan la reacción de división del agua. Pero para entender por qué necesitamos conocer los motivos clave a escala atómica ".
Hasta donde ellos saben, los científicos son los primeros en estudiar la titania amorfa a una escala tan fina.
"Para comprender la evolución estructural de la titania a nivel atómico, necesitábamos científicos que supieran cómo cultivar materiales activos, cómo caracterizar estos materiales con las herramientas que existen en el CFN y NSLS-II, y cómo dar sentido a los resultados de la caracterización aprovechando las herramientas teóricas, "dijo Stavitski.
Próximo, El equipo ampliará su enfoque de combinar el análisis de datos de espectroscopía experimental y teórico a materiales relevantes para la ciencia de la información cuántica (QIS). El campo emergente de QIS aprovecha los efectos cuánticos en física, o los comportamientos e interacciones extraños que ocurren a escalas ultrapequeñas. Esperan que los usuarios de CFN y NSLS-II hagan uso del enfoque en otros campos de investigación, como el almacenamiento de energía.