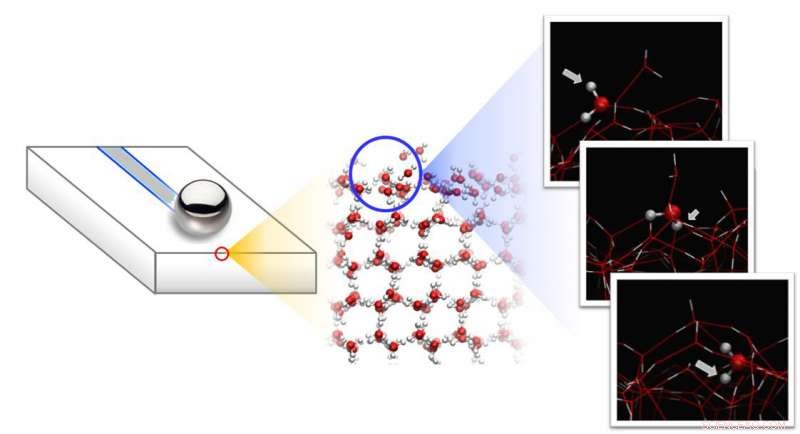
En los experimentos, una bola de acero se desliza sobre la superficie del hielo, que consiste en moléculas de agua móviles que giran rápidamente y que solo están unidas ligeramente al hielo subyacente. Crédito:Nagata / MPI-P
Deportes de invierno como el esquí, patinaje de velocidad, patinaje artístico y el rizado requieren superficies resbaladizas de hielo y nieve. Si bien se reconoce ampliamente el hecho de que la superficie del hielo es resbaladiza, está lejos de entenderse completamente. En 1886 John Joly, un físico irlandés, ofreció la primera explicación científica de la baja fricción en el hielo; cuando un objeto, es decir, un patín de hielo, toca la superficie del hielo, la presión de contacto local es tan alta que el hielo se derrite creando una capa de agua líquida que lubrica el deslizamiento. El consenso actual es que, aunque el agua líquida en la superficie del hielo reduce la fricción por deslizamiento sobre el hielo, esta agua líquida no se derrite por presión sino por el calor de fricción producido durante el deslizamiento.
Un equipo de investigadores dirigido por los hermanos Prof.Daniel Bonn de la Universidad de Amsterdam y Prof. Mischa Bonn de MPI-P, Ahora han demostrado que la fricción sobre el hielo es más compleja de lo que se suponía hasta ahora. A través de experimentos macroscópicos de fricción a temperaturas que oscilan entre 0 ° C y -100 ° C, los investigadores muestran que, sorprendentemente, la superficie del hielo se transforma de una superficie extremadamente resbaladiza a las temperaturas típicas de los deportes de invierno. a una superficie con alta fricción a -100 ° C.
Para investigar el origen de este deslizamiento dependiente de la temperatura, los investigadores realizaron mediciones espectroscópicas del estado de las moléculas de agua en la superficie, y los comparó con simulaciones de dinámica molecular (MD). Esta combinación de experimento y teoría revela que existen dos tipos de moléculas de agua en la superficie del hielo:moléculas de agua que están pegadas al hielo subyacente (unidas por tres enlaces de hidrógeno) y moléculas de agua móviles que están unidas por solo dos enlaces de hidrógeno. Estas moléculas de agua móviles ruedan continuamente sobre el hielo, como pequeñas esferas, impulsadas por vibraciones térmicas.
A medida que aumenta la temperatura, las dos especies de moléculas de superficie se interconvierten:el número de moléculas de agua móviles aumenta a expensas de las moléculas de agua que se fijan a la superficie del hielo. Notablemente, este cambio impulsado por la temperatura en la movilidad de las moléculas de agua más altas en la superficie del hielo coincide perfectamente con la dependencia de la temperatura de la fuerza de fricción medida:cuanto mayor es la movilidad en la superficie, cuanto menor sea la fricción y viceversa. Por lo tanto, los investigadores concluyen que, en lugar de una fina capa de agua líquida sobre el hielo, la alta movilidad de las moléculas de agua de la superficie es responsable de la resbaladiza del hielo.
Aunque la movilidad de la superficie continúa aumentando hasta los 0 ° C, esta no es la temperatura ideal para deslizarse sobre hielo. Los experimentos muestran que la fricción es mínima a -7 ° C; se impone exactamente la misma temperatura en las pistas de patinaje de velocidad. Los investigadores muestran que a temperaturas entre -7 ° C y 0 ° C, deslizarse es más difícil porque el hielo se vuelve más blando, haciendo que el objeto deslizante se hunda más profundamente en el hielo.
Los resultados se publican en el Revista de letras de química física .