Gráficamente abstracto. Crédito:célula molecular (2022). DOI:10.1016/j.molcel.2022.07.007
Durante más de un siglo, el metabolismo de las células cancerosas se ha visto como una especie de paradoja. Un nuevo trabajo de investigadores de la Universidad de Washington en St. Louis muestra que, después de todo, podría no ser una anomalía tan grande. El estudio se publica el 15 de agosto en Molecular Cell.
La glucosa, un azúcar común en los alimentos, es uno de los nutrientes más importantes del cuerpo. Las células cancerosas tienden a consumirlo a un ritmo asombroso. A primera vista, parece tener sentido porque las células cancerosas tienen mucho trabajo de síntesis. Después de todo, como los tumores crecen rápidamente, cada célula tiene que replicar todo su contenido.
Pero aquí está el truco. Las células cancerosas no utilizan la glucosa de manera muy eficiente. En lugar de absorber toda la energía que pueden de la glucosa, liberan la mayor parte como material de desecho.
"Para extraer la máxima cantidad de energía de la glucosa, las células deben transportar sus productos de transformación a las mitocondrias", dijo Gary Patti, profesor Michael y Tana Powell de Química en Artes y Ciencias y de genética y medicina en la Facultad de Medicina. Patti, miembro del Centro de Cáncer Siteman en el Hospital Barnes-Jewish y la Facultad de Medicina, es la autora principal del nuevo estudio
"Hay ciertas reglas bioquímicas que se supone que debe seguir el metabolismo. Ha sido interesante pensar en por qué los tumores podrían romperlas", dijo Patti. "Sin embargo, los hallazgos que informamos aquí demuestran que las células cancerosas siguen los principios convencionales".
Desbordante
Las mitocondrias son pequeños compartimentos dentro de las células, a menudo denominados centrales eléctricas o centrales eléctricas de la célula. Lo que entra y sale de ellos está estrictamente controlado.
Como un poco de historia de fondo, un famoso bioquímico llamado Otto Warburg descubrió por primera vez la naturaleza derrochadora de los tumores en la década de 1920. Para explicar por qué no se extrae más energía de la glucosa, postuló que las mitocondrias están dañadas en las células cancerosas.
"Ahora sabemos que esto no es cierto. Las mitocondrias son funcionales y, de hecho, activas en la mayoría de los cánceres", dijo Patti. Pero eso deja sin respuesta una pregunta persistente e inquietante:¿Por qué las células cancerosas metabolizan tan poca glucosa que consumen en las mitocondrias?
"Creo que lo que ha sido confuso es que ha existido la noción de que las células cancerosas prefieren no oxidar la glucosa en sus mitocondrias", dijo Patti. "Tal vez como un legado del pensamiento original de Warburg o tal vez porque sucede tan ampliamente, a menudo se ha asumido que las células cancerosas quieren usar la glucosa de manera derrochadora".
Se han ofrecido todo tipo de explicaciones sobre por qué las células cancerosas podrían querer derrochar su glucosa. Sin embargo, Patti y su equipo sostienen que estas racionalizaciones pueden ser innecesarias. Al final, el metabolismo del cáncer puede no ser tan inusual como pensaban los científicos.
Las células cancerosas realmente quieren metabolizar la glucosa en sus mitocondrias, y lo hacen. Hasta que no puedan.
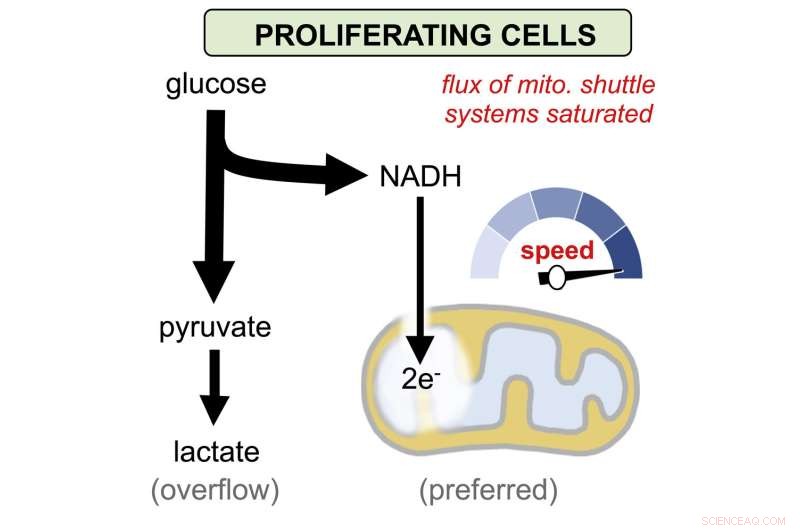
"Cuando restringimos la cantidad de glucosa absorbida por las células cancerosas, casi toda llega a las mitocondrias", dijo Patti. "Pero a medida que aumenta el consumo de glucosa, la velocidad de movimiento de las moléculas derivadas de glucosa hacia las mitocondrias no puede mantenerse".
En otras palabras, las células cancerosas solo desperdician glucosa porque el transporte a las mitocondrias es demasiado lento.
Imagine un grifo de la bañera que escupe agua más rápido de lo que el desagüe puede sacarla. Eventualmente, el agua se desborda en el piso.
"Este no es un paradigma metabólico radicalmente nuevo. La mayoría de las células prefieren oxidar la glucosa en las mitocondrias en lugar de excretarla como desecho", dijo Patti. "Nuestros datos sugieren que las células cancerosas no son una excepción. Parecen seguir los mismos patrones bioquímicos que otras células".
Saturado
El descubrimiento del equipo de Patti fue posible gracias a una poderosa tecnología llamada metabolómica.
"Durante la última década, los avances en el campo de la metabolómica y la espectrometría de masas han sido extraordinarios", señaló Patti. "Hemos llegado a un punto en el que incluso es posible medir moléculas en células individuales".
En este estudio, los investigadores combinaron la metabolómica con trazadores de isótopos estables. Esto les permitió etiquetar diferentes partes de la glucosa para poder rastrearla dentro de las células, observando la velocidad a la que las cosas ingresaban a las mitocondrias o se excretaban de las células. Así es como los científicos descubrieron que las vías normales para el transporte de combustible se estaban superando o saturando en las células cancerosas.
La velocidad a la que los tumores consumen glucosa ha sido explotada por médicos en la clínica durante décadas como una forma de diagnosticar el cáncer e identificar su etapa. También ha llevado a algunos a creer que limitar la absorción de glucosa con medicamentos o con una dieta sin azúcar podría "matar de hambre" a las células cancerosas.
Los hallazgos de este estudio plantean preguntas sobre dicha estrategia.
"Es posible que tengamos que repensar cuál es la mejor manera de abordar el metabolismo de la glucosa en el cáncer", dijo Patti. "Si las células cancerosas absorben más glucosa de la que necesitan, y su uso derrochador no es un impulsor de la enfermedad, entonces el metabolismo de la glucosa puede no ser un objetivo terapéutico tan atractivo como esperábamos". El cáncer tiene un efecto dominó en los tejidos distantes