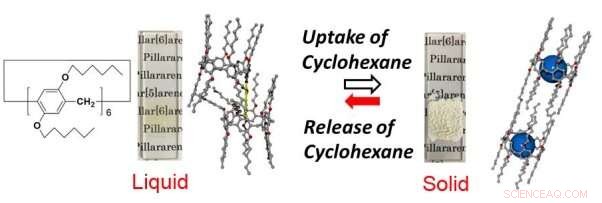
Figura 1. Ilustración esquemática del cambio de estado inducido por el vapor invitado de ciclohexano del pilar [6] areno con 12 grupos n-hexilo. Crédito:Universidad de Kanazawa
El cambio reversible de moléculas macrocíclicas entre una fase líquida y una sólida tras la exposición al vapor se ha informado en el Revista de la Sociedad Química Estadounidense por investigadores de la Universidad de Kanazawa.
La transición entre una fase sólida y una líquida, un proceso clave en la vida diaria y la ciencia de los materiales, generalmente es impulsado por un cambio de temperatura o presión. Sin embargo, También es posible un cambio de estado reversible causado por otros estímulos:por ejemplo, la luz se ha utilizado para inducir transiciones sólido-líquido.
Tomoki Ogoshi de la Universidad de Kanazawa en Japón y sus colegas estudiaron moléculas pilar [n] areno, moléculas en forma de pilar que fueron reportadas por primera vez por su grupo de investigación, a las que se pueden agregar grupos funcionales para modificar sus propiedades físicas. Introduciendo 12 n-hexil (C 6 H 13 ) las cadenas en las moléculas transforman el sistema en un líquido estructural a temperatura ambiente, es decir, un sistema con un cierto grado de orden a nanoescala pero sin una estructura periódica (Figura 1) .El líquido se solidifica cuando se expone a un vapor invitado, cuyas moléculas reemplazan los sustituyentes n-hexilo en las cavidades de las moléculas en forma de pilar. Al mismo tiempo, los sustituyentes ubicados fuera de las cavidades cristalizan. El resultado es que, en una escala de tiempo de unos segundos, el sistema solidifica y el líquido transparente cambia a un sólido turbio.
Como vapor invitado competitivo, los autores utilizaron ciclohexano, porque encaja en las cavidades de las moléculas en forma de pilar y es fácil de quitar calentando la muestra a presión reducida, un proceso que da como resultado que el sistema molecular vuelva al estado líquido. Los procesos de adsorción y desorción se caracterizan por mediciones de resonancia magnética nuclear, mientras que la estructura del sistema se estudia mediante difracción de rayos X.
Los autores también investigaron la absorción de otros vapores orgánicos por el líquido estructural, observando que la exposición a moléculas que podrían ser absorbidas en los poros de las moléculas en forma de pilar siempre resultó en una transición a una fase sólida, mientras que la transición de fase no se observó para la exposición a gases que tuvieran una baja absorción por el líquido estructural.
Este sistema se puede utilizar como detector de vapores de alcanos, un dispositivo inusual. "Debido a la selectividad del vapor, postulamos que el cambio de estado inducido por vapor puede aplicarse a nuevos sistemas de detección de vapor, "comentan los autores." Otra aplicación son los materiales de adhesión que utilizan el cambio de estado inducido por el vapor invitado ".
Fondo
Química huésped-huésped:la química supramolecular es una rama de la química que estudia los sistemas químicos compuestos por varias moléculas, describiendo su interacción, que son esenciales para muchos procesos biológicos. Las interacciones huésped-huésped son un ejemplo:este es el tipo de interacción que funciona cuando una molécula huésped forma un compuesto químico con una molécula huésped o ión sin la participación de enlaces covalentes. Este tipo de interacción se puede aprovechar, por ejemplo, en sistemas de administración de fármacos en los que la presencia del huésped aumenta la solubilidad y la disponibilidad del fármaco (el huésped).
Pillararenos:moléculas de macrociclo que toman su nombre de su forma de pilar. Las cavidades de estas moléculas pueden albergar moléculas pobres en electrones. Algunas de estas moléculas tienen potencial para aplicaciones biomédicas, sino también para la absorción de gases, líquidos iónicos y materiales orgánicos emisores de luz.